Hibrid sp3
Hibridisasi menjelaskan atom-atom yang berikatan dari sudut pandang sebuah atom. Untuk sebuah karbon yang berkoordinasi secara tetrahedal (seperti metana, CH4), maka karbon haruslah memiliki orbital-orbital yang memiliki simetri yang tepat dengan 4 atom hidrogen. Konfigurasi keadaan dasar karbon adalah 1s2 2s2 2px1 2py1 atau lebih mudah dilihat: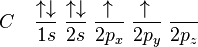
(Perhatikan bahwa orbital 1s memiliki energi lebih rendah dari orbital 2s, dan orbital 2s berenergi sedikit lebih rendah dari orbital-orbital 2p)
Teori ikatan valensi memprediksikan, berdasarkan pada keberadaan dua orbital p yang terisi setengah, bahwa C akan membentuk dua ikatan kovalen, yaitu CH2. Namun, metilena adalah molekul yang sangat reaktif (lihat pula: karbena), sehingga teori ikatan valensi saja tidak cukup untuk menjelaskan keberadaan CH4.
Lebih lanjut lagi, orbital-orbital keadaan dasar tidak bisa digunakan untuk berikatan dalam CH4. Walaupun eksitasi elektron 2s ke orbital 2p secara teori mengijinkan empat ikatan dan sesuai dengan teori ikatan valensi (adalah benar untuk O2), hal ini berarti akan ada beberapa ikatan CH4 yang memiliki energi ikat yang berbeda oleh karena perbedaan aras tumpang tindih orbital. Gagasan ini telah dibuktikan salah secara eksperimen, setiap hidrogen pada CH4 dapat dilepaskan dari karbon dengan energi yang sama.
Untuk menjelaskan keberadaan molekul CH4 ini, maka teori hibridisasi digunakan. Langkah awal hibridisasi adalah eksitasi dari satu (atau lebih) elektron:
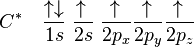
Proton yang membentuk inti atom hidrogen akan menarik salah satu elektron valensi karbon. Hal ini menyebabkan eksitasi, memindahkan elektron 2s ke orbital 2p. Hal ini meningkatkan pengaruh inti atom terhadap elektron-elektron valensi dengan meningkatkan potensial inti efektif.
Kombinasi gaya-gaya ini membentuk fungsi-fungsi matematika yang baru yang dikenal sebagai orbital hibrid. Dalam kasus atom karbon yang berikatan dengan empat hidrogen, orbital 2s (orbital inti hampir tidak pernah terlibat dalam ikatan) "bergabung" dengan tiga orbital 2p membentuk hibrid sp3 (dibaca s-p-tiga) menjadi
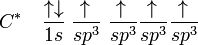
Pada CH4, empat orbital hibrid sp3 bertumpang tindih dengan orbital 1s hidrogen, menghasilkan empat ikatan sigma. Empat ikatan ini memiliki panjang dan kuat ikat yang sama, sehingga sesuai dengan pengamatan.
 sama dengan
sama dengan 
Sebuah pandangan alternatifnya adalah dengan memandang karbon sebagai anion C4−. Dalam kasus ini, semua orbital karbon terisi:

Jika kita menrekombinasi orbital-orbital ini dengan orbital-s 4 hidrogen (4 proton, H+) dan mengijinkan pemisahan maksimum antara 4 hidrogen (yakni tetrahedal), maka kita bisa melihat bahwa pada setiap orientasi orbital-orbital p, sebuah hidrogen tunggal akan bertumpang tindih sebesar 25% dengan orbital-s C dan 75% dengan tiga orbital-p C. HaL ini sama dengan persentase relatif antara s dan p dari orbital hibrid sp3 (25% s dan 75% p).
Menurut teori hibridisasi orbital, elektron-elektron valensi metana seharusnya memiliki tingkat energi yang sama, namun spektrum fotoelekronnya menunjukkan bahwa terdapat dua pita, satu pada 12,7 eV (satu pasangan elektron) dan saty pada 23 eV (tiga pasangan elektron). Ketidakkonsistenan ini dapat dijelaskan apabila kita menganggap adanya penggabungan orbital tambahan yang terjadi ketika orbital-orbital sp3 bergabung dengan 4 orbital hidrogen.





Tidak ada komentar:
Posting Komentar